已有的研究表明,蛙類歪頭病的致病因子為細菌,目前已經從各類病蛙中鑒定出十幾株病原菌,包括:米爾伊麗莎白菌(Elizabethkingia miricola)、腦膜膿毒性伊麗莎白菌(E. meningoseptica)、肺炎克雷伯菌(Klebsiella pneumoniae)、醋酸鈣不動桿菌(Acinetohacter calcoaceticus)等,并以伊麗莎白菌屬最為常見。這些菌株多為多重耐藥菌,其中一些菌株(如米爾伊麗莎白菌)與人類臨床分離株(可引起新生兒腦膜炎)具有較高的親緣關系。當前,雖然對于歪頭病致病因子的鑒定工作取得了一定進展,但其病理機制卻極少有研究,且我們對于健康蛙類所攜帶的本底病原菌的豐度及其潛在感染途徑等均不了解,這些研究的空缺使得養殖蛙類歪頭病 的防治工作遲遲無法取得進展。
的防治工作遲遲無法取得進展。
為此,中國科學院成都生物研究所江建平研究團隊的朱未、常利明和趙春霖調查了四川境內養殖黑斑蛙(俗稱青蛙)的歪頭病爆發情況。發現疾病爆發的蛙場內至少存在兩種類型的病蛙:其中一種僅表現出歪頭的癥狀,其運動平衡喪失,大量溺死;另一種同時表現出歪頭、白內障和浮腫等癥狀,繼而于陰暗處病死(圖1)。通過比較無癥狀個體、歪頭個體和“歪頭+白內障”個體的腦、眼球和消化道菌群發現,米爾伊麗莎白菌是這些病蛙的致病因子,其在兩種病蛙的腦中均具有很高的豐度,而僅在“歪頭+白內障”個體的眼球中具有高豐度。所有個體的消化道菌群中米爾伊麗莎白菌的豐度極低,說明其從消化道感染黑斑蛙的可能性較低。值得注意的是,多種其他類型的歪頭病致病菌亦存在于養殖黑斑蛙的體表或腸道中,雖然其不是此次疾病爆發的致病因子,但是卻有引起歪頭病爆發的潛在可能。
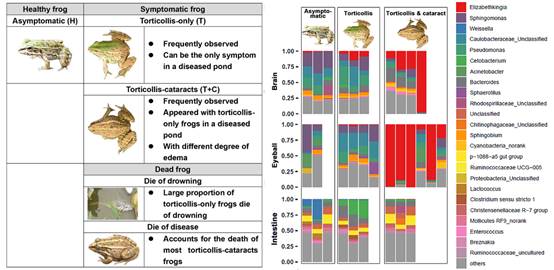
圖1 不同癥狀的病蛙和微生物組成分析
組織病理學分析發現,歪頭個體表現出明顯的腦膜血管充血,而“歪頭+白內障”個體還額外表現出明顯的軟腦膜淋巴細胞滲透以及中樞神經系統損傷;兩種病蛙均出現肝臟脂肪儲備降低的現象。病蛙與無癥狀個體的主要基因表達差異存在于腦組織中,且這些差異基因主參與免疫反應,病蛙表現出免疫識別(NOD-like receptor signaling pathway and Toll-like receptor signaling pathway)、發炎反應(TNF signaling pathway and Cytokine-cytokine interaction)和適應性免疫應答(B cell receptor signaling pathway)的全面激活。兩類病蛙的基因表達在腦組織和肝臟中存在明顯差異。在腦組織中,“歪頭+白內障”個體表現出強烈的天然免疫和炎癥應答,且急性期蛋白的轉錄水平顯著升高;在肝臟中,“歪頭+白內障”個體同樣表現出更顯著的急性期蛋白表達上調和能量代謝基因下調。這些結果共同提示兩種病蛙處于腦部感染的不同病理階段。結合人細菌性腦膜炎的病程,我們推測歪頭個體處于軟腦膜侵入和感染的早期,還未引發腦膜炎;由于未發現歪頭個體的肌肉存在明顯的病理和基因轉錄變化,因此我們推測歪頭癥狀和運動失衡可能是源于神經系統感染。而在“歪頭+白內障”個體中,感染已經引起腦膜炎,其所伴隨的系統性發炎可導致“血眼屏障”的突破(眼部感染)和組織水腫,進而解釋了為何“白內障”癥狀的出現可以預測腦膜炎的發生(圖2)。
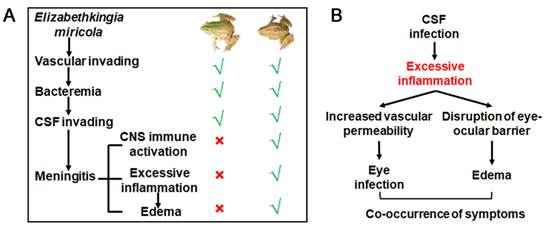
圖2 典型癥狀的病理機制
基于這些結果,我們為歪頭病的預防提出以下幾點建議:
1.出現歪頭癥狀時病原菌已入侵腦膜,抗生素治療所導致的細菌裂解可能促進炎癥反應,加速病蛙的死亡,因此該疾病應以預防為主;
2.由于多種致病菌被黑斑蛙正常攜帶,監測黑斑蛙體表及養殖環境的微生物組成和豐度或可預測歪頭病暴發的風險;
3.有研究表明兩棲動物在暴露于某些滅活的病原物之后仍可獲得免疫記憶,而伊麗莎白菌感染可激活黑斑蛙的適應性免疫,我們或可嘗試使用滅活病原菌暴露的方式提前激活黑斑蛙對該病原菌的的免疫能力。
該研究得到了中國科學院戰略先導研究項目(XDA19050201), 國家自然科學基金項目(31900327), 中國科學院西部之光人才培養項目(2016XBZG_XBQNXZ_B_008), 以及四川省科技廳基礎條件平臺建設項目(2019JDPT0020)的支助。近日,這項工作以常利明為第一作者,題為 “Microbiomic and transcriptomic insight into the pathogenesis of meningitis-like disease in cultured Pelophylax nigromaculatus”發表于水產領域經典期刊Aquaculture。
